전이 암세포의 생존 메커니즘이 발견됐다.
육종인 연세대 교수와 황금숙 한국기초과학지원연구원 박사 연구팀은 암이 처음 발생한 장기에서 다른 조직으로 퍼져나가는 '전이 과정' 중 암세포가 어떻게 생존하고, 대사 경로를 바꾸는지 메커니즘을 최초로 규명했다고 21일 밝혔다. 대사는 세포에서 생명을 유지하기 위해 일어나는 화학 반응이다.
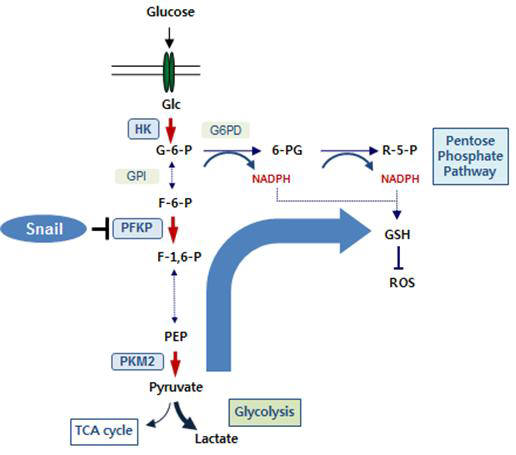
연구팀은 암세포가 주변 조직을 공격해 뻗어 나가는 것은 암세포 스스로 특정 단백질 '스네일(Snail)'을 이용해 대사물질(PFKP)을 억제해 대사를 조절하면서 이뤄진다는 것을 확인했다.
암세포는 포도당 공급이 없는 기아 상태의 대사 스트레스를 극복하고 살아남기 위해 스네일 을 이용해 탄수화물이 세포 내 이동할 때 주로 포도당 형태로 이동하는 당대사경로 흐름을 재조정한다. 산소 존재 유무에 상관없이 포도당을 젖산으로 바꾸는 당대사경로인 호기성 해당작용(aerobic glycolysis)을 억제하고 포도당 6-인산을 리불로즈 5-인산으로 산화시키는 5탄당 인산경로(PPP)를 활성화시키는 방향으로 포도당 대사경로 흐름이 바뀐다.
전이 과정의 암세포는 스네일이 당대사경로에서 호기성 해당작용과 5탄당 인산경로 스위치 역할을 하는 PFKP를 억제시켜 암세포가 생존할 수 있는 환원력을 얻는다는 사실을 발견했다.
전이 암세포가 대사 조절의 핵심 물질로 이용한 것이 PFKP라는 사실은 동물실험에서도 확인됐다. 동물 전이 모델에서 암유전자인 스네일은 폐 전이를 증가시키고, 여기에 PFKP를 증가시키면 다시 폐 전이가 억제됐다. 연구팀은 스네일이 PFKP 발현을 억제해 암세포 생존능력을 증가시키고 생체 내에서 암 전이를 유도하는 것을 보여주는 결과라고 설명했다.
육종인 교수는 “6년 연구 끝에 나온 이번 성과는 그동안 연구가 전무했던 전이 과정의 암세포 대사 조절에 대한 최초 연구 보고로, 전이되는 암세포는 증식하는 암세포와 달리 이화작용 쪽으로 대사를 조절해 생존한다는 것을 밝혔다”면서 “새로운 대사 치료표적을 제공해 대사경로 타깃으로 알려진 기존 대사약제를 암 치료에 적용할 수 있는 근거를 제공할 것”으로 기대했다.
연구 결과는 학술지 네이처 커뮤니케이션즈(Nature Communications) 2월 8일자에 게재됐다.
송혜영기자 hybrid@etnews.com