개발자를 위한 의료기기 소프트웨어(SW) 안정성 가이드라인이 처음 개발된다. 선진국 중심으로 의료기기 SW 인증이 의무화된 가운데, 대응에 어려움을 겪는 중소 의료기기 기업 대상이다. 인공지능(AI) 등 SW 만으로 구성된 의료기기가 출시된 상황에서 안정성, 유효성을 담보할 지침서가 된다.
정보통신산업진흥원(NIPA)과 연세의료원은 '의료기기 SW SIL(Safety Integrity Level)-B 가이드라인'을 연말 발간한다고 13일 밝혔다. 가이드라인은 의료기기에 탑재되는 SW 안정성과 유효성을 담보하기 위해 설계, 개발, 검증 전 과정에 확인해야 할 주요사항을 제시한다. 의료기기 위험관리 표준 ISO14971, SW 관련 표준 IEC62304 등을 기반으로 한다.
SIL 등급은 A·B·C 세 등급으로 나뉜다. 이번 개발하는 B 등급은 SW 오작동으로 생명에 위협을 가하지는 않지만 환자 안전에 중대한 위험을 내포하는 수준이다. 의료기기 SW 오작동 대부분이 B 등급에 해당한다.
기존 식품의약품안전처 의료기기 SW 가이드라인은 인·허가 지원을 위한 것이다. 이번 가이드라인은 결과물이 아닌 개발 초기부터 실무진이 체크해야 할 부분을 상세히 제시한다. 인·허가 필수 기술문서 작성에 참고할 첫 개발자용 가이드라인이다.
한태화 연세의료원 산학융합의료센터 교수는 “가이드라인은 인·허가만이 목적이 아니라 국제표준 이해와 주변 환경, 규제 등을 포괄적으로 이해시키고 개발하는 참고서”라면서 “안정성, 유효성 기반 기술문서를 작성하게 돕는 가이드라인”이라고 말했다.
전자 신호로 진단, 검사, 처리하는 의료기기가 늘면서 SW 중요성이 커진다. 최근 AI 등 SW 만으로 이뤄진 진단지원 의료기기까지 출시됐다. 환자 생명에 중대한 영향을 미치는 의료기기 특성상 SW 오류는 치명적이다. 방사선 치료기기 '테라크-25' SW 오류로 3명이 사망하고 3명은 심각한 방사능 후유증에 시달린 것이 대표 사례다.
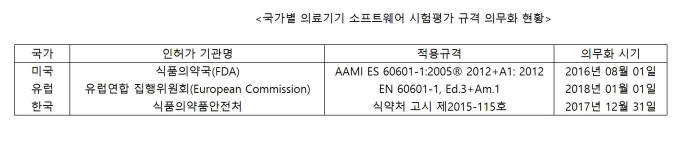
선진국 중심으로 의료기기 인·허가 과정에서 SW 시험평가를 의무화한다. 미국 식품의약국(FDA)는 2016년 8월부터 국제표준규격 기반 SW 시험평가인 'AAMI ES 60601-1'을 강제화했다. 유럽연합(EU) 집행위원회는 올해부터 'EN 60601-1'을 의무화했다. 우리나라도 작년 말부터 전자의료기기 기준 규격에 따라 IEC 60601-1, IEC 62304를 따르도록 했다. 의료기기 인증을 받을 때 SW도 의무적으로 안정성, 유효성을 검증 받아야 한다.
국내 의료기기 업계 대응은 뒤처진다. 하드웨어(HW) 중심 의료기기 산업 구조가 고착화됐다. 연 매출 10억원 미만 기업이 전체 80% 이상을 차지하는 영세성도 한몫한다. 대부분 SW 개발은 외주를 주기 때문에 문제 발생 시 대응이 어렵다. 자칫 수출 길마저 좁아질 우려다.
NIPA와 연세의료원은 올 연말까지 가이드라인을 개발해 온·오프라인 배포한다. SW공학현장적용사업을 실시해 가이드라인을 기반으로 컨설팅 사업을 시작한다. 연세의료원은 의공학팀, 의료기기임상시험센터 등 의료기기 기업과 접점이 있는 부서 대상으로 가이드라인 배포·확산 사업을 펼친다. 원주의료기기테크노밸리 등 의료기기 클러스터와 협업도 모색한다.
한 교수는 “설문조사 결과 의료기기 기업 90%가 SW 표준, 시험평가 규정 등을 인지하지만, 대부분 개발 업무는 외주를 줘 전문 지식이 부족한 상황”이라면서 “성능을 담보할 의료기기 SW를 개발해 글로벌 시장 진출을 도울 것”이라고 말했다.
[전자신문 CIOBIZ] 정용철 의료/바이오 전문기자 jungyc@etnews.com