
네오이뮨텍이 미국 보건당국과 접촉하며 급성방사선증후군(ARS) 치료제의 정부 전략 물자 편입을 타진한다. 개발 중인 치료제의 최종 임상을 앞두고 매출 기반을 미리 확보한다는 전략에서다.
네오이뮨텍은 오는 11일(현지시간) 미국 보건복지부 산하 생물의학첨단연구개발국(BARDA)과 '테크와치' 미팅을 갖는다. 네오이뮨텍의 T 세포 증폭제 'NT-I7'의 ARS 림프구 치료제로서 개발 현황과 허가 전략을 공유하고, 미국 정부 비축 프로그램 편입 가능성과 협력 방안 등을 논의한다.
이번 미팅은 정부 조달 체계를 통한 공급이 주요 상업화 경로가 되는 ARS 치료제 특성 때문이다. ARS는 단시간에 방사선에 대량 노출돼 면역체계가 손상되는 질환이다. 미국 정부는 생화학 무기 위협 등에 대비해 ARS 치료제를 전략 물자로 비축한다. 앞서 미국 식품의약국(FDA) 승인을 받은 ARS 치료제 역시 정부 대상 매출이 꾸준히 발생하고 있다.
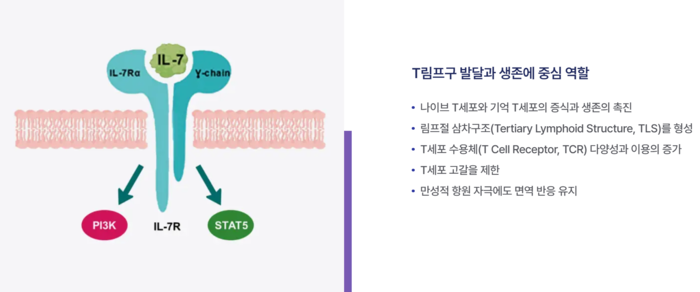
네오이뮨텍은 정부 전략 물자 개발과 조달을 담당하는 BARDA와 협력을 모색한다. NT-I7은 세포 면역을 담당하는 림프구를 늘려 증상을 치료한다. 혈소판과 호중구 수치를 높이는 방식으로 접근한 기존 4개 ARS 치료제와 차이가 있다. 신약 승인만 된다면 NT-I7 구매 수요가 존재할 것으로 보고, 이번 미팅에서 임상 효과와 허가 가능성 등을 공유할 계획이다.
네오이뮨텍은 NT-I7의 최종 동물실험 설계를 위한 FDA 미팅도 지난해 말 가졌다. 1차 영장류 실험에서 NT-I7 고용량 투여군은 전신 방사선에만 노출된 위약 대조군 대비 생존율이 43%포인트(P) 향상됐다. 기존 ARS 치료제의 38~43%P 생존율 개선 효과와 유사하다.
네오이뮨텍은 두 번째 영장류 실험에서 NT-I7의 치료 효능을 입증하고 신약 허가에 도전한다. ARS 치료제는 윤리적 문제로 인간 대상 임상시험을 할 수 없어, 두 가지 이상 동물종에서 효능을 입증해 품목 허가를 받는다. 이번 실험을 위해 FDA와 사전 미팅을 거친 만큼 빠른 임상 진행을 기대할 수 있다.
네오이뮨텍 관계자는 “FDA 허가 전략과 정부 협력을 병행해 ARS 치료제 개발과 상업화 기반을 단계적으로 구축하겠다”고 말했다.
송윤섭 기자 sys@etnews.com









