서울대병원이 에임넥스트를 미국 식품의약국(FDA) 허가용 확증 임상시험 지원 대상으로 선정했다고 12일 밝혔다. 국내 슬립테크 의료기기의 해외 임상 지원에 착수했다.
이번 임상 지원은 산업통상부 '바이오나노산업 개방형생태계 조성사업' 세부 과제인 '인공지능(AI) 기반 슬립테크 국제협력 실증 확산 지원'에 따라 추진한다. 해외에서는 임상 근거를 기반으로 한 슬립테크 제품의 표준화와 글로벌 시장 진출이 본격화됐지만, 국내 슬립테크 산업은 임상 검증과 국제 실증 경험이 제한적인 상황을 보완하기 위해 사업이 마련됐다.
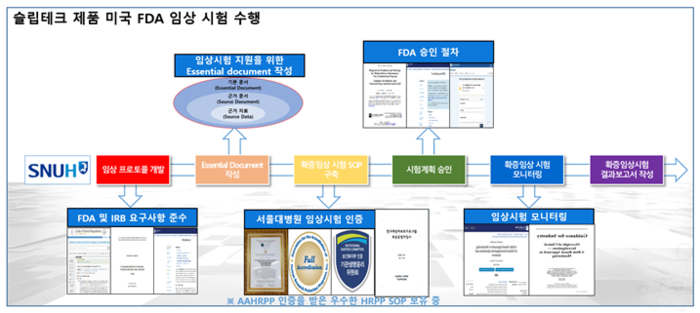
서울대병원은 수면 질환 예방·진단·치료 분야 AI 기반 슬립테크 의료기기를 대상으로 미국 FDA 허가를 목표로 한 확증 임상이 국제 기준에 맞게 수행되도록 지원하고 있다. 미국 FDA, 유럽 의료기기 규정 'CE MDR' 허가용 확증 임상을 중심으로 시험계획서 개발, 기본 문서 작성, 사전검토, 현지 승인 절차 지원, 수행 관리와 품질 점검 등을 돕는다. 서울대병원은 주관기관으로서 슬립테크 의료기기의 임상시험 전반을 총괄한다.
이번에 선정된 에임넥스트는 국내 1호 디지털 치료기기(DTx)인 불면증 치료용 애플리케이션 '솜즈'를 개발했다. 에임넥스트는 이번 지원을 받아 미국 임상을 준비한다. 유럽 임상 지원은 올해 하반기 공고에서 별도 모집한다.
연구책임자인 이유진 서울대병원 수면의학센터장(정신건강의학과 교수)은 “AI 기반 슬립테크와 디지털 치료기기는 해외 허가 과정에서 임상적 근거와 국제 기준 충족이 중요하다”면서 “서울대병원은 주관기관으로서 슬립테크 의료기기의 임상 검증과 해외 임상시험 수행을 체계적으로 지원하고 있다”고 말했다.
송윤섭 기자 sys@etnews.com









