
글로벌 인공지능(AI) 헬스케어 시장에서 각국이 AI 알고리즘 변경 관리와 고위험 AI 규제 체계 정비에 속도를 내고 있다. 한국도 생성형 AI에 맞춘 심사·사후관리 고도화 등이 필요하다는 지적이다.
한국보건산업진흥원이 최근 발간한 '글로벌 인공지능 헬스케어 산업 동향과 규제 변화' 보고서에 따르면 글로벌 AI 헬스케어 시장이 2023년 224억달러(약 32조9593억원)에서 2030년 1880억달러(약 276조원) 규모로 확대될 것으로 전망했다. 시장 성장에 맞춰 AI 활용 영역도 다중모달 AI, 자율형 에이전트, 원격 환자 모니터링(RPM), 디지털 치료기기(DTx) 등으로 확장되고 있다.
AI 활용 영역이 넓어지면서 규제 쟁점도 제품 허가 단계에서 허가 이후 관리로 이동하고 있다. 특히 AI 의료기기는 알고리즘 업데이트와 학습데이터 보완을 통해 성능이 달라질 수 있어, 주요국은 허가 이후 변경 범위와 검증 방식, 사후 모니터링 기준을 제도화하는 데 속도를 내고 있다.
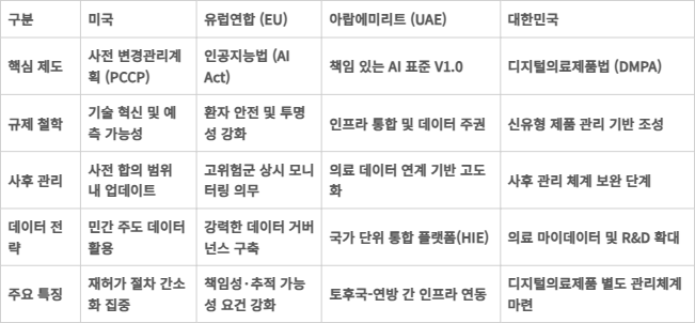
미국은 AI 의료기기 변경관리 체계를 제도화하는 대표 사례로 꼽힌다. 미 식품의약국(FDA)은 AI 알고리즘이 지속적으로 변화할 수 있는 특성을 고려해 '사전 변경관리계획(PCCP)'을 도입했다. 기존 규제에서는 AI 성능을 고도화할 때 추가 허가 또는 변경 절차 부담이 발생할 수 있었다. 그러나 PCCP를 적용하면 제조사가 사전에 합의한 '알고리즘 변경 범위'와 '검증 방식' 내에서는 별도 심사 부담을 줄이면서 제품 업데이트가 가능해진다. 이는 AI의 지속적인 성능 개선을 제도권 안에서 관리하려는 조치로, 기업의 제품 개선 속도를 뒷받침하면서 규제 당국의 심사 부담을 줄일 수 있는 모델로 평가된다.
아랍에미리트(UAE)는 7개 토후국으로 구성된 연방제 국가 행정 특성을 반영해 의료 데이터 인프라를 구축하고 있다. 아부다비 '말라피', 두바이 '나비드', 연방 차원의 '리아야티' 등을 통해 의료 데이터 연계 기반을 고도화하고, 데이터 주권 정책과 '책임 있는 AI 표준 V1.0'을 병행하는 모습이다.
반면 유럽연합(EU)은 인공지능법(AI Act)으로 AI 헬스케어 기기 등 고위험 시스템 규제 강화에 나섰다. 의료 AI는 환자 안전과 직결되는 만큼 데이터 품질·투명성·사후 모니터링을 의무화해 시장 진입부터 운영 전반에서 책임성과 추적 가능성을 요구하는 흐름이다.
한국은 최근 디지털의료제품법 시행을 통해 AI 소프트웨어 등 신유형 의료제품 관리 기반을 마련했다. 다만 AI 의료기기 허가 후 변경관리 체계, 특히 생성형 AI 의료기기에 대한 관리 기준은 구체화가 필요한 영역으로 꼽힌다.
생성형 AI 기기는 학습데이터, 환각 가능성, 업데이트 방식 등에서 기존 기기와 달라 실제 현장에서 성능 저하나 편향 문제가 발생할 때를 대비한 모니터링 기준이 필요하다. 성능 변경 시 이를 어느 범위까지 추가 승인 없이 허용하고 통제할 것인지에 대한 세부 가이드라인 보완이 필요하다는 지적이다.
업계 한 관계자는 “AI 헬스케어 경쟁 축이 규제 예측 가능성 확보로 옮겨가고 있다”며 “한국도 생성형 AI 특성에 맞춘 심사·사후관리 가이드라인을 구체화해 기술 변화를 제도적으로 뒷받침해야 할 필요성이 커지고 있다”고 말했다.
임중권 기자 lim9181@etnews.com









