
바이오니아(대표 박한오)는 자회사 써나젠테라퓨틱스가 개발한 신약후보물질(SAMiRNA-AREG)에 대한 검증시험 계약을 해외 제약회사와 맺었다고 19일 밝혔다.
후보물질을 제공받은 해외 제약회사는 전문 업체에 실험을 맡겨 치료 효과를 검증한 뒤 최종 보고서를 제출하게 된다.
검증시험은 물질이전 계약과 함께 통상적으로 신약 기술이전 과정 중 하나로 꼽힌다.
검증시험 데이터와 최종보고서 등 연구 결과물에 대한 소유권과 지식재산권은 써나젠테라퓨틱스가 갖는다.
써나젠테라퓨틱스는 이 후보물질에 대해 식품의약품안전처에 연내 1상 임상시험을 신청할 계획이다.
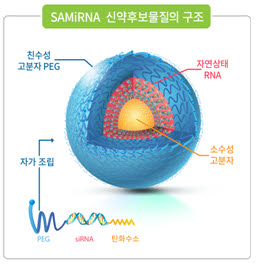
'SAMiRNA'는 질병 mRNA를 분해하는 siRNA(짧은 간섭 RNA)가 인체에서 쉽게 분해되지 않고 타깃 세포까지 전달돼 약효를 오래 유지하도록 양 끝에 각각 친수성·소수성 물질을 결합한 단일분자 신약 플랫폼이다.
80~90㎚ 크기에 수용액에서 저절로 중성 전하를 띤 공 모양 나노입자를 형성하기 때문에 인체 면역세포가 이물질로 인식하지 못한다.
바이오니아와 써나젠테라퓨틱스는 전 세계 원천특허와 후보물질 특허 등 190여건 지식재산권을 보유하고 있다.
국내에서 이뤄진 다양한 질환 모델 동물실험 및 영장류 독성시험에서 만성 신장질환, 원인을 알 수 없는 특발성 폐섬유증, 비알코올성 지방간염(NASH) 등 염증·섬유증 억제 효과와 안정성도 입증된 바 있다. 반면 선천 면역반응 같은 부작용은 나타나지 않았다.
바이오니아 관계자는 “후보물질 모델링이 단순해 검증시험 결과 도출까지는 기간이 길지 않을 것”이라며 “비밀유지 조항으로 상세한 계약 내용을 밝힐 수는 없지만 후보물질이 글로벌 시장으로 나아가는 디딤돌이 될 것”이라고 말했다.
대전=이인희기자 leeih@etnews.com









